문제
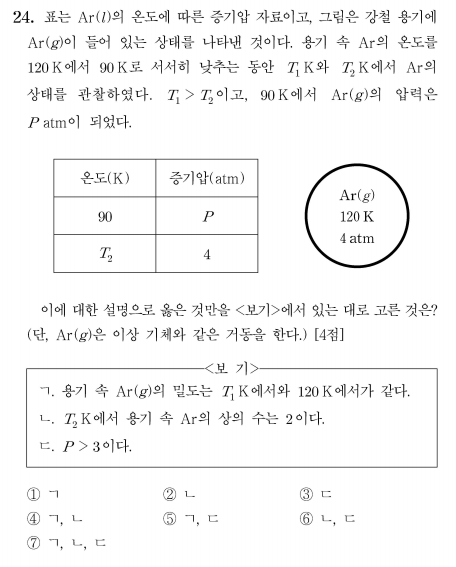
위와 같이 강철 용기 내에 기체 상태를 알려주고 온도를 낮추며 증기압을 측정한다는 상황을 알려주고, 각 지점에서의 온도 또는 증기압을 물어보는 문제를 풀어봅시다.
풀이

우선 문제에서 주어진 조건을 가지고 최대한 정보를 이끌어내면, 먼저 120K의 온도에서 기체가 모두 증발한 상황에서 4atm임을 알 수 있고, 온도를 120K에서 낮추면서 T_1, T_2를 거쳐 90K가 되므로 위와 같은 부등식을 만들 수 있습니다.
그리고 120K의 Ar이 모두 기체인 조건에서 4atm이라고 하였으므로 더 낮은 온도인 T_2에서 증기압만으로 4atm의 압력을 만들려면 T_2에서도 Ar은 모두 기체여야 합니다.
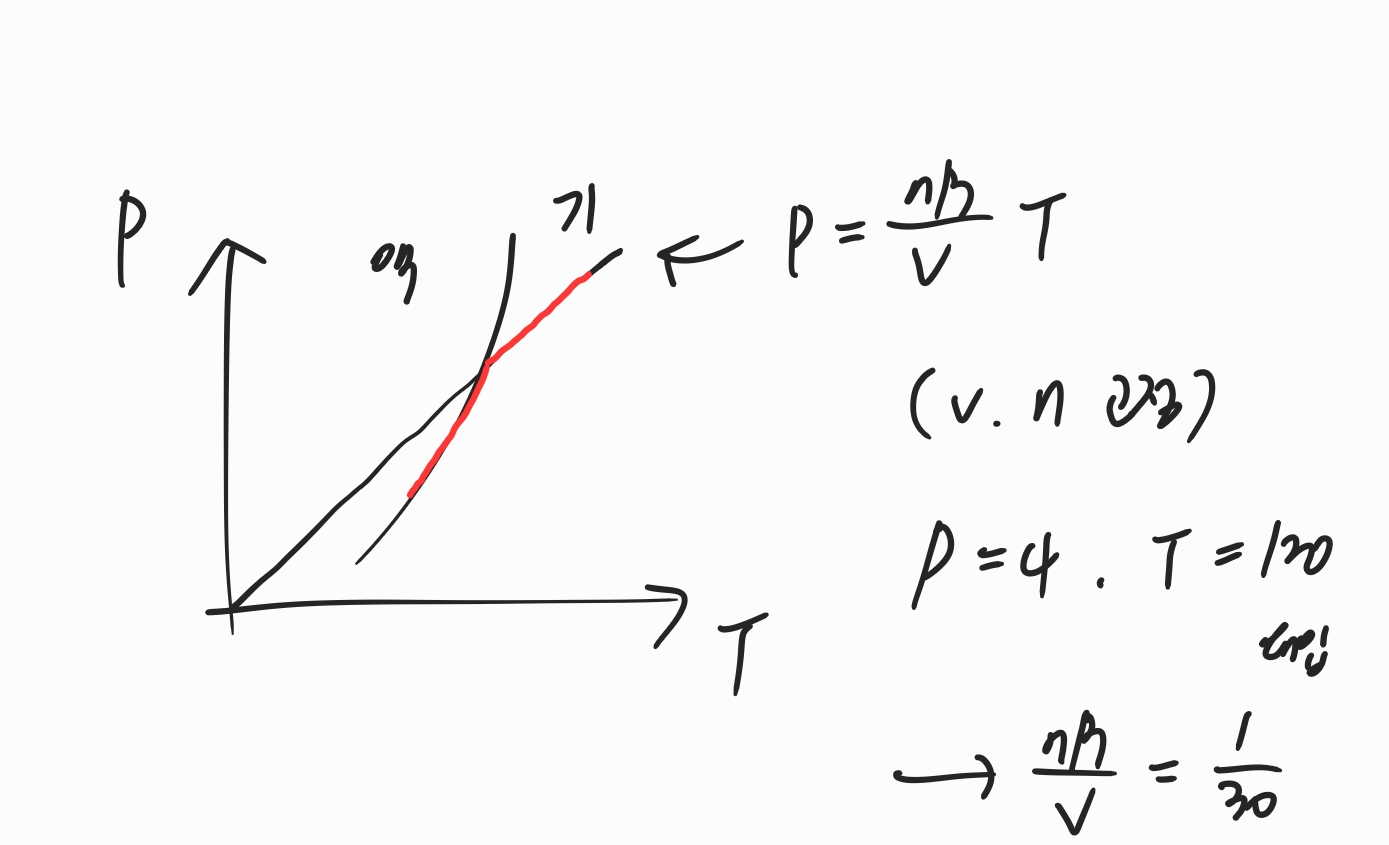
그래프를 예상하여 그려보면 위와 같은 상평형 그래프를 P=nR/V * T의 직선형 그래프가 지나간다는 것을 예상할 수 있습니다. (이 때 강철 용기이므로 V는 고정이고 반응이 일어나지도 않으므로 n 또한 고정입니다.)
그리고 120K에서 4atm이라고 하였으므로 P와 T를 대입해보면 그래프의 기울기는 1/30임을 알 수 있습니다.

온도가 바뀌면 당연히 P가 같이 바뀌기 때문에 역으로 P가 같다면 같은 온도일 수밖에 없습니다. 따라서 T_2는 120K이고 문제에서 주어진 부등식에 의해 둘의 온도 사이에 있던 T_1 또한 120K가 되어야합니다.
저는 이것이 문제오류라고 생각하는데, 사실 120K에서 아주 미세하게 차이가 있다고 가정하면 부등식이 성립하는게 틀린 말도 아니기는 합니다.
어쨌든 위와 같은 결론을 가지고 보기를 확인해보면 온도가 같으므로 기체의 밀도 또한 같을 수 밖에 없습니다. 따라서 보기 ㄱ은 맞습니다.

그 다음 보기 ㄴ에서는 T_2에서 Ar의 상은 2개가 존재한다고 하였는데 4atm이므로 모두 기체상태로 존재해야 합니다. (상평형의 위치에 있어도 오직 1가지 상만으로 존재할 수 있습니다.) 따라서 보기 ㄴ은 틀렸습니다.

보기 ㄷ의 경우 90K에서의 압력이 3atm보다 크다고 하였는데, 아까 위에서 그린 그래프를 살펴보면 기화 그래프가 직선 그래프보다 아래에 있으므로 압력은 항상 1/30 T보다 작거나 같습니다. 따라서 아까 구한 기울기와 T = 90K라는 조건을 대입하면 압력은 항상 3atm 이하임을 알 수 있고 따라서 보기 ㄷ은 틀렸음을 알 수 있습니다.
따라서 맞는 보기는 ㄱ뿐이고 정답은 1번입니다.
저는 개인적으로 이 문제의 온도 부등식 설정에 오류가 있다고 생각하는데, 혹시 이 문제에 관련하여 제 풀이에 틀린 점이 있다거나 2018학년도 시험에서 문제오류가 있었다는 내용을 알고계신 분은 댓글로 알려주신다면 반영하여 수정하도록 하겠습니다.
'자연과학(PEET) > 일반화학' 카테고리의 다른 글
| [기체] 피스톤으로 압축한 후 생성물의 몰수를 구하는 문제 (2020학년도 11번) (0) | 2021.02.28 |
|---|---|
| [화학 평형] 수용액 pH를 변화시킬 때 물질 농도 구하는 문제 (2021학년도 25번 풀이) (0) | 2021.02.28 |
| [상평형] 평형점을 주고 온도를 변화시켜 일부 승화시키는 문제 (2015학년도 21번 풀이) (0) | 2021.02.27 |
| [증기압] 액체가 섞인 실린더에서 압력을 구하는 문제 (2016학년도 8번 풀이) (0) | 2021.02.27 |
| [증기압] Clausius-Clapeyron 식을 이용한 그래프 해석 문제 (2014학년도 21번 풀이) (0) | 2021.02.27 |