반응식

알켄에 RCO3H를 처리하면 에폭사이드를 생성하는 반응을 만들 수 있습니다. 이 때 RCO3H의 R로는 다양한 분자식이 들어갈 수 있으며, HCO3H와 mCPBA가 대표적입니다. 기타 위에 적혀있는 분자식들이나 물질도 에폭시화반응에 사용이 가능합니다.
예시

아주 간단한 형태의 반응식으로 위와 같은 예시가 있습니다. 알켄에 RCO3H를 처리하면 알켄의 이중결합이 깨지고 RCO3H에서도 결합이 깨지면서 새로운 산소 삼각고리가 만들어지는 것을 확인할 수 있습니다.

메커니즘이 규명되어있기는 하지만, 굳이 어떤 산소가 떨어져나오는지 그 과정을 알 필요는 없고, 대략적으로 위의 그림에 해당하는 부분이 반응하며, 결과물로 에폭사이드와 함께 RCOOH(카르복실산)이 떨어져나온다는 점만 알면 됩니다.
예제

위의 반응식은 어떤 생성물을 결과로 나타낼지 예상해봅시다.

정답은 위와 같고, 그 이유는 왼쪽으로 산소가 첨가될 경우 steric이 커서 불안정한 생성물이 얻어지기 때문입니다. 따라서 steric이 비교적 적은 오른쪽에 산소가 첨가되어 위와 같은 생성물이 얻어짐을 예상해볼 수 있습니다.

위의 반응식은 어떤 생성물이 얻어질지 예상해봅시다. 왼쪽 알켄에 첨가될지 오른쪽 알켄에 첨가될지뿐만이 아니라 syn 첨가인지 anti 첨가인지 또한 예상해보라는 말입니다.

정답은 오른쪽 알켄에 첨가이며, anti 첨가가 진행됩니다. 먼저 왼쪽이 아닌 이유는, 위의 반응은 첨가 과정의 전이 상태에서 EDG가 필요한 반응이기 때문에, 왼쪽의 2치환 알켄보다는 오른쪽의 3치환 알켄이 전이상태에서 더욱 안정하고, 따라서 오른쪽 이중결합에 산소가 첨가되는 것을 예상해볼 수 있습니다. 그리고 anti 첨가가 일어나는 이유는 위의 예제에서도 확인해보았듯 steric 때문입니다.
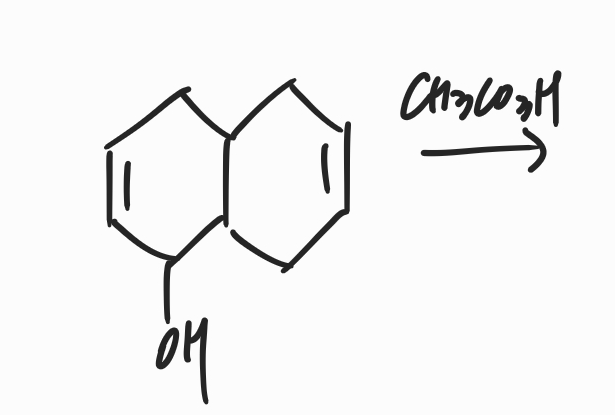
위의 반응식에 대한 생성물을 예측해보세요. 위와 같은 이유로 예제를 둔 것은 아닙니다. 반응 위치에 대한 또다른 근거를 생각해보세요.

정답은 위와 같습니다. OH는 EDG가 아닌 EWG이기 때문에, 왼쪽 알켄에서 반응할 경우 전이상태에서 시그마 결합을 통한 전자 제공이 충분하지 않아 오른쪽보다 불안정합니다. 따라서 오른쪽 알켄에서 반응이 일어나 오른쪽과 같은 에폭사이드가 형성됩니다. (참고로 아래쪽으로 산소가 첨가될 수도 있습니다. 따라서 라세미 혼합물이 만들어지겠네요.)

위와 같은 반응식의 경우 어떤 생성물이 나타날지 예상해봅시다. 이 예제 역시 위와 같은 이유로 둔 것은 아니니 잘 생각해보세요. (syn 첨가일지 anti 첨가일지를 예상해보라는 문제)

정답은 syn 첨가입니다. 그 이유는 뭘까요? 위의 그림에 나타난대로 전이상태에서 산소가 수소와 수소결합을 형성하기 때문에 steric보다도 안정해지는 효과가 더 크기 때문입니다. 따라서 syn 첨가가 일어납니다. steric만 가지고 예상했다면 틀렸을 것입니다.
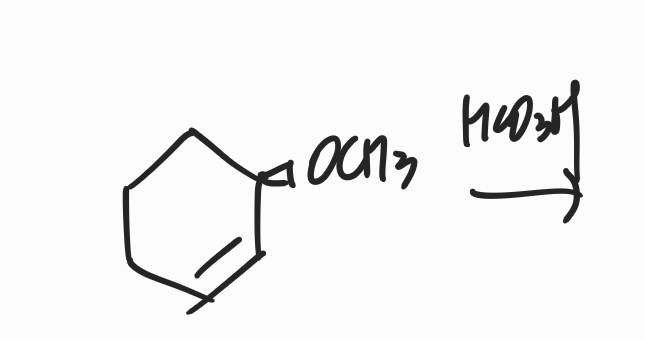
위와 같은 반응식의 생성물을 예상해보세요. 이번에는 steric과 수소결합 모두를 고려하여 어떤 효과가 더 클 것인지 예상해야합니다.

정답은 위와 같습니다. 역시 수소가 있기 때문에 수소결합을 할 수도 있을 것이라고 예상할 수 있는데, OCH3에서는 수소가 산소와 직접적으로 연결된 것도 아니고 (시그마 결합을 통해 전하를 끌어당기는 효과가 훨씬 약해짐) 따라서 수소 결합력이 더 약할 것이며 무엇보다도 OH에 비해 OCH3는 steric이 더 커지기 때문에 위와 다르게 anti 첨가가 일어날 것으로 예상할 수 있습니다.
물론 두 가지 효과가 상충되는 경우 어느 쪽의 효과가 무조건 강하다고 확신할 순 없지만, 직관적인 예측을 통해 최대한 정답에 가까운 결과를 예상하는 것이 중요합니다. 물론 그보다 더 좋은 방법은 미리미리 여러 가지 예제를 통해 어떤 효과가 어떨 때 더 강한지 최대한 많은 경우의 수를 파악하는 것입니다.
'자연과학(PEET) > 유기화학' 카테고리의 다른 글
| [알켄] 가오존분해반응 (Ozonolysis) (+ 생성물 쉽게 외우는 법) (0) | 2021.02.13 |
|---|---|
| [알켄] 하이드록시화반응 (Hydroxylation) (0) | 2021.02.13 |
| [알켄] 금속촉매수소첨가반응 (Hydrogenation) (0) | 2021.02.13 |
| [알켄] Simmons-Smith 반응 (+ Carbenoid 합성법) (0) | 2021.02.12 |
| [알켄] Cyclepropane 합성반응 (+ Carbene 합성법) (0) | 2021.02.12 |