2020학년도 1번


아세트산은 약산이고 이를 강염기로 적정하는 상황이므로 당량점에 도달하면 염기성 용액이 됩니다.
따라서 염기성 pH를 변색 범위로 가지고 있는 페놀프탈레인 시약을 사용해야합니다.
아세트산의 몰농도는 MV = 일정 공식을 사용하면 20mL임을 알 수 있습니다.
따라서 정답은 4번입니다.
2020학년도 6번


몰농도와 몰랄농도에 대해서 묻는 문제입니다.
몰농도는 용액 부피에 반비례하고, 밀도 또한 용액 부피에 반비례하므로 몰농도의 비와 밀도 비는 같습니다.
따라서 M2/M1 = d2/d1이므로 M2 = M1 * d2/d1이고, M1 = 1이므로 (나) 용액의 몰농도는 d2/d1입니다.
그 다음 몰랄농도는 용액 질량에서 용질 질량을 빼주어야 하므로 분모에 d2 - 0.04가 들어가게 됩니다.
이를 계산해주면 (나) 용액의 몰랄 농도는 25 / (25d1 - 1)임을 알 수 있습니다.
따라서 정답은 2번입니다.
2020학년도 7번


약산 HA를 강염기 NaOH로 적정하는 상황에서의 적정 그래프에 대해 묻는 문제입니다.
반응 용액의 종류는 총 2가지가 있는데, 0.1M 10mL와 0.01M 100mL의 약산입니다.
두 용액에 들어있는 HA의 총 몰수는 같으나, 부피가 다른 경우이므로 부피가 더 큰 쪽이 pH가 덜 변할 것입니다.
이를 이용해 보기의 그래프를 살펴보면, 산성 염기성 범위 모두에서 pH 변화가 덜 나타나는 그래프는 1번과 5번입니다.
그런데 5번 그래프는 산성 범위에서 NaOH 첨가에 따라 pH가 오히려 더 많이 차이나는 효과가 있으므로 정답이 아닙니다.
따라서 정답은 1번입니다.
2020학년도 11번

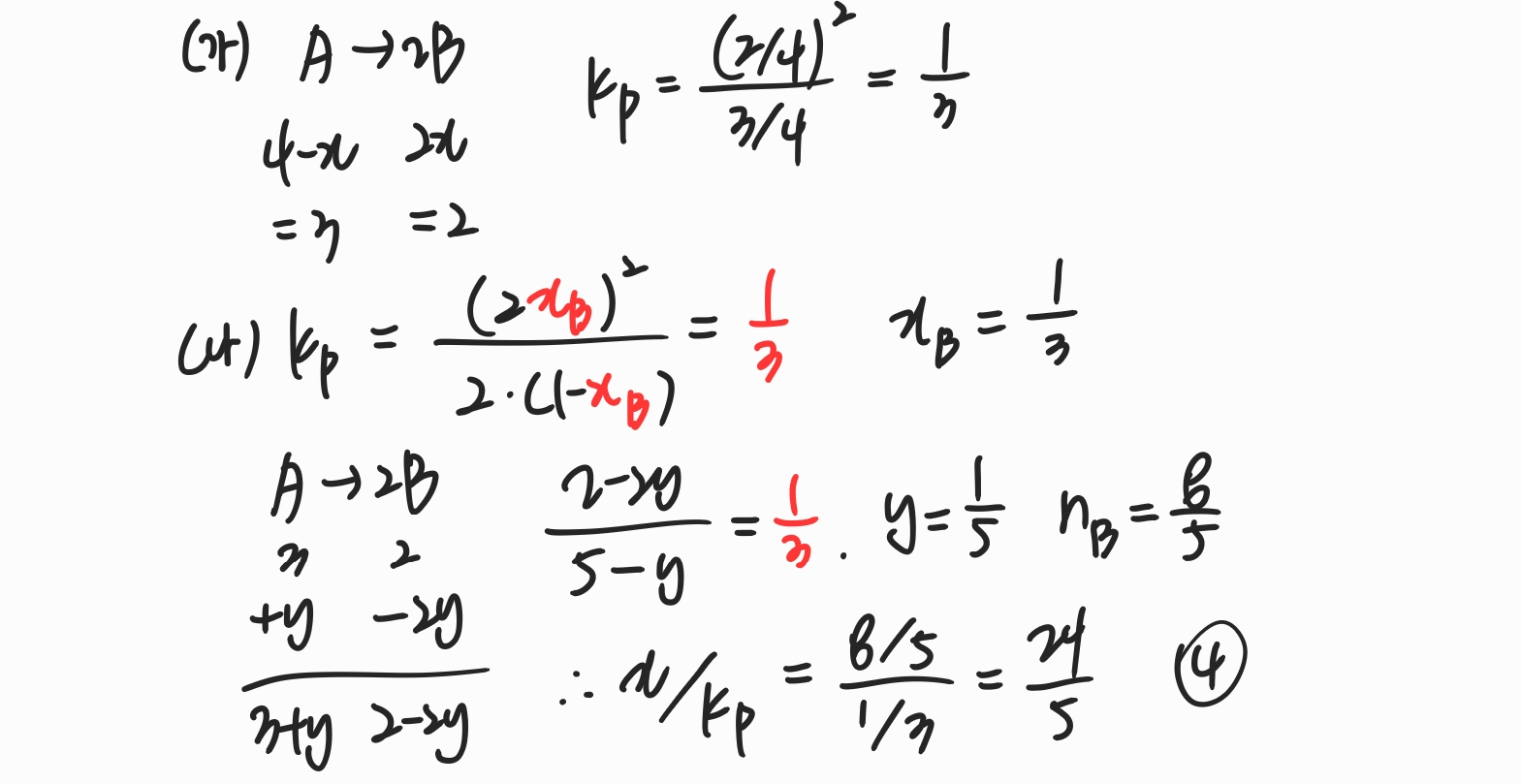
기체 반응과 평형 상수에 대한 문제입니다.
초기 A 몰수는 4mol이고, 반응 후 3mol이 되었으므로 이를 이용해 반응한 몰수와 평형 상수를 계산할 수 있습니다.
그러면 K_p = 1/3임을 알 수 있습니다.
그 다음 (나)에서 새로운 평형에 도달하는데 이 때 압력은 기체 몰수에 비례하므로 이를 이용해 식을 세우고 K_p를 이용하여 반응 몰수를 구해야 합니다.
그런데 그냥 x로 두고 계산할 경우 식이 아주 복잡해지기 때문에, 여기서 미지수를 잘 두어야 합니다.
가장 편한 방법은 분자 제곱 항에 x^2이 위치하도록 하는 것이므로, 그러기 위해서 B의 몰분율을 미지수로 둡니다.
그러면 간단하게 x_B = 1/3을 구할 수 있고, 따라서 나중 B의 몰수 x = 8/5임을 알 수 있습니다.
따라서 문제에서 물어본 x / K_p = 24/5이고, 정답은 4번입니다.
2020학년도 20번


ㄱ. 깁스 자유에너지 값 자체가 생성물의 자유에너지가 반응물의 자유에너지에 비해 어떻게 변화하는지를 나타내는 값이므로 △G 값이 0보다 크다면 생성물의 깁스 에너지가 더 크다는 것이므로 맞습니다.
ㄴ. (가) 상황이 평형 상태이므로 표준 깁스 자유에너지 값이 0이 되게 하는 T 값을 구하면 됩니다.
위의 식대로 계산하면 T = 1050이므로 보기 ㄴ은 틀렸습니다.
ㄷ. △G_dot = -RTlnK이므로 여기에 적절한 값들을 대입하고, kJ과 J 단위를 맞춰주고 확인하면 보기의 식과 부호가 다르므로 보기 ㄷ은 틀렸음을 알 수 있습니다.
따라서 정답은 1번입니다.
2020학년도 21번


여러 반응식들의 용해도곱상수에 대한 문제입니다.
ㄱ. 문제 상황 자체가 물에서 반응이 일어나는 것이 아닌 NH3에 용해시키는 과정이므로 AgI + 2NH3 → Ag(NH3)2+ + I- 반응식의 K 값을 구해야 합니다.
주어진 식들로 적절히 K 값을 구하고 이를 바탕으로 용해도를 구하면 s = 4 × 10^(-5)이므로 보기 ㄱ은 맞습니다. (위의 풀이에서 숫자를 잘못 적음)
ㄴ. (나)에서 NaBr을 투입하면 AgBr의 침전에 Ag가 소모되므로 I-가 증가합니다.
이 때 Ag+는 감소하지만 AgI의 분해량이 증가하고, 이는 곧 AgI의 몰 용해도가 증가함을 의미하므로 보기 ㄴ은 맞습니다.
ㄷ. (나)에 AgI를 추가해도 K_sp 값에 AgI의 농도는 반영되지 않으므로 변화 없습니다.
따라서 정답은 4번입니다.
2020학년도 24번


전기 화학 파트 문제입니다.
ㄱ. 수소 전극에 대한 네른스트 식을 작성해보면 위와 같이 되고, 이 때 log[H+]가 x축 값이므로 log[H+] 꼴을 만들어주어야 합니다.
수소 전극의 네른스트 식을 적절히 조정해서 만들어주면 기울기가 0.06이 나오고, 비슷한 방식으로 전극 I의 네른스트 식에서 기울기 값이 같다고 두면 m = 1이므로 보기 ㄱ은 맞습니다.
ㄴ. a-b 값이 0보다 커야 자발적으로 반응이 일어날 것이므로, 전극 II가 산화 전극임을 알 수 있습니다.
ㄷ. 보기 ㄷ의 식을 만들기 위해 전체 반응식의 네른스트 식을 만들어주면, 위와 같은 식이 나오고 이 값을 비교하면 보기 ㄷ에서 제시한 식과 부호가 다르므로 틀렸습니다.
따라서 정답은 1번입니다.
'자연과학(PEET) > 일반화학' 카테고리의 다른 글
| [PEET 일반화학] 2011학년도 1회 PEET 일반화학 고난도 기출문제 풀이/해설 (0) | 2021.07.17 |
|---|---|
| [PEET 일반화학] 2021학년도 11회 PEET 일반화학 고난도 기출문제 풀이/해설 (0) | 2021.07.08 |
| [PEET 일반화학] 2019학년도 9회 PEET 일반화학 고난도 기출문제 풀이/해설 (0) | 2021.07.08 |
| [PEET 일반화학] 2018학년도 8회 PEET 일반화학 고난도 기출문제 풀이/해설 (0) | 2021.06.06 |
| [전기화학] 반쪽 반응식 두 개와 전위 그래프를 주고 미지수를 찾는 문제 (2013학년도 13번 풀이) (1) | 2021.03.08 |